Progreso e análise económica da produción de hidróxeno por electrólise de óxidos sólidos
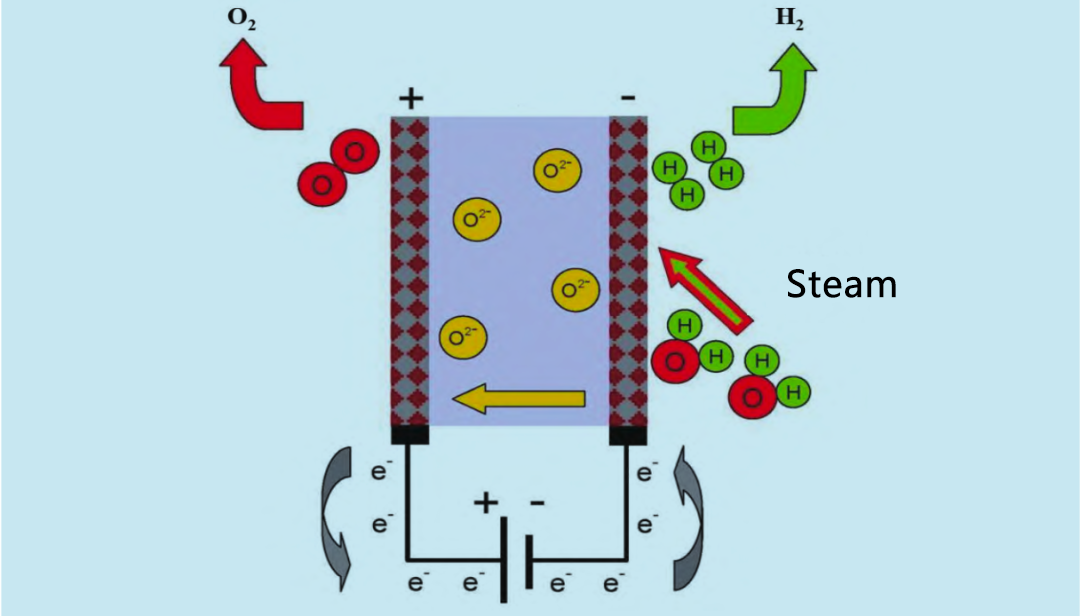
O electrolizador de óxido sólido (SOE) usa vapor de auga a alta temperatura (600 ~ 900 °C) para a electrólise, o que é máis eficiente que o electrolizador alcalino e o electrolizador PEM. Na década de 1960, Estados Unidos e Alemaña comezaron a investigar o SOE con vapor de auga a alta temperatura. O principio de funcionamento do electrolizador SOE móstrase na Figura 4. O hidróxeno reciclado e o vapor de auga entran no sistema de reacción desde o ánodo. O vapor de auga electrolízase en hidróxeno no cátodo. O O2 producido polo cátodo móvese a través do electrolito sólido ata o ánodo, onde se recombina para formar osíxeno e liberar electróns.
A diferenza das células electrolíticas de membrana alcalinas e de intercambio de protóns, o eléctrodo SOE reacciona co contacto de vapor de auga e enfróntase ao desafío de maximizar a área de interface entre o eléctrodo e o contacto de vapor de auga. Polo tanto, o eléctrodo SOE xeralmente ten unha estrutura porosa. O propósito da electrólise de vapor de auga é reducir a intensidade enerxética e o custo operativo da electrólise convencional da auga líquida. De feito, aínda que o requisito total de enerxía da reacción de descomposición da auga aumenta lixeiramente co aumento da temperatura, o requisito de enerxía eléctrica diminúe significativamente. A medida que aumenta a temperatura electrolítica, parte da enerxía requirida subministrase en forma de calor. O SOE é capaz de producir hidróxeno en presenza dunha fonte de calor a alta temperatura. Dado que os reactores nucleares arrefriados por gas a alta temperatura poden quentarse a 950 °C, a enerxía nuclear pode utilizarse como fonte de enerxía para o SOE. Ao mesmo tempo, a investigación demostra que a enerxía renovable, como a enerxía xeotérmica, tamén ten o potencial como fonte de calor da electrólise de vapor. O funcionamento a alta temperatura pode reducir a tensión da batería e aumentar a velocidade de reacción, pero tamén enfronta o desafío da estabilidade térmica e o selado do material. Ademais, o gas producido polo cátodo é unha mestura de hidróxeno, que precisa ser separada e purificada aínda máis, o que aumenta o custo en comparación coa electrólise convencional da auga líquida. O uso de cerámicas condutoras de protóns, como o circonato de estroncio, reduce o custo do SOE. O circonato de estroncio mostra unha excelente condutividade de protóns a uns 700 °C e favorece que o cátodo produza hidróxeno de alta pureza, o que simplifica o dispositivo de electrólise de vapor.
Yan et al. [6] informaron de que se empregou un tubo cerámico de circona estabilizado con óxido de calcio como SOE da estrutura de soporte, a superficie exterior estaba revestida con perovskita de lantano porosa fina (menos de 0,25 mm) como ánodo e cermet de óxido de calcio estable de Ni/Y2O3 como cátodo. A 1000 °C, 0,4 A/cm2 e 39,3 W de potencia de entrada, a capacidade de produción de hidróxeno da unidade é de 17,6 NL/h. A desvantaxe do SOE é a sobretensión resultante das altas perdas de ohmios que son comúns nas interconexións entre as celas e a alta concentración de sobretensión debido ás limitacións do transporte por difusión de vapor. Nos últimos anos, as celas electrolíticas planas chamaron moita atención [7-8]. En contraste coas celas tubulares, as celas planas fan que a fabricación sexa máis compacta e melloran a eficiencia da produción de hidróxeno [6]. Na actualidade, o principal obstáculo para a aplicación industrial do SOE é a estabilidade a longo prazo da cela electrolítica [8], e poden causar problemas de envellecemento e desactivación dos eléctrodos.
Data de publicación: 06-02-2023