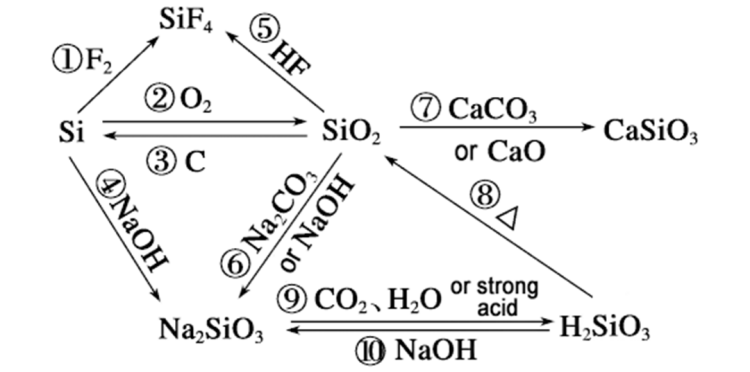
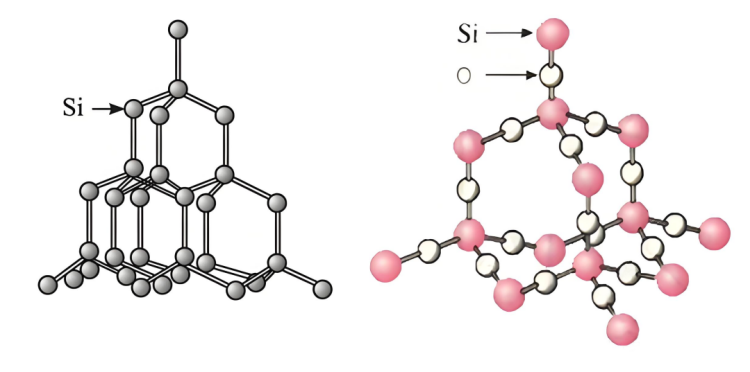
Чаму хуткасць рэакцыікрэмнійі гідраксід натрыю можа пераўзыходзіць дыяксід крэмнію, што можна прааналізаваць з наступных бакоў:
Розніца ў энергіі хімічнай сувязі
▪ Рэакцыя крэмнію і гідраксіду натрыю: Калі крэмній рэагуе з гідраксідам натрыю, энергія сувязі Si-Si паміж атамамі крэмнію складае ўсяго 176 кДж/моль. Падчас рэакцыі сувязь Si-Si разрываецца, і яе адносна лягчэй разарваць. З кінетычнага пункту гледжання рэакцыя працякае лягчэй.
▪ Рэакцыя дыяксіду крэмнію і гідраксіду натрыю: энергія сувязі Si-O паміж атамамі крэмнію і атамамі кіслароду ў дыяксіде крэмнію складае 460 кДж/моль, што адносна высока. Для разрыву сувязі Si-O падчас рэакцыі патрабуецца большая энергія, таму рэакцыя адбываецца адносна цяжка, а хуткасць рэакцыі павольная.
Розныя механізмы рэакцыі
▪ Крэмній рэагуе з гідраксідам натрыю: спачатку крэмній рэагуе з гідраксідам натрыю, утвараючы вадарод і крэмніевую кіслату, а затым крэмніевая кіслата рэагуе з гідраксідам натрыю, утвараючы сілікат натрыю і ваду. Падчас гэтай рэакцыі паміж крэмніем і вадой вылучаецца цяпло, якое можа спрыяць руху малекул, тым самым ствараючы лепшае кінетычнае асяроддзе для рэакцыі і паскараючы хуткасць рэакцыі.
▪ Дыяксід крэмнію рэагуе з гідраксідам натрыю: спачатку дыяксід крэмнію рэагуе з гідраксідам натрыю, утвараючы крэмніевую кіслату, а затым крэмніевая кіслата рэагуе з гідраксідам натрыю, утвараючы сілікат натрыю. Рэакцыя паміж дыяксідам крэмнію і вадой надзвычай павольная, і працэс рэакцыі практычна не вылучае цяпла. З кінетычнага пункту гледжання, гэта не спрыяе хуткай рэакцыі.
Розныя матэрыяльныя структуры
▪ Структура крэмнію:Крэмніймае пэўную крышталічную структуру, і існуюць пэўныя прамежкі і адносна слабыя ўзаемадзеянні паміж атамамі, што палягчае кантакт і рэакцыю раствора гідраксіду натрыю з атамамі крэмнію.
▪ Структуракрэмнійдыяксід:крэмнійдыяксід мае стабільную прасторавую сеткавую структуру.КрэмнійАтамы крэмнію і атамы кіслароду цесна звязаны кавалентнымі сувязямі, утвараючы цвёрдую і стабільную крышталічную структуру. Раствору гідраксіду натрыю цяжка пранікнуць унутр і цалкам звязацца з атамамі крэмнію, што абцяжарвае хуткую рэакцыю. Толькі атамы крэмнію на паверхні часціц дыяксіду крэмнію могуць рэагаваць з гідраксідам натрыю, што абмяжоўвае хуткасць рэакцыі.
Уплыў умоў
▪ Рэакцыя крэмнію з гідраксідам натрыю: пры награванні хуткасць рэакцыі крэмнію з растворам гідраксіду натрыю значна паскараецца, і рэакцыя, як правіла, можа працякаць гладка пры высокіх тэмпературах.
▪ Рэакцыя дыяксіду крэмнію з гідраксідам натрыю: Рэакцыя дыяксіду крэмнію з растворам гідраксіду натрыю пры пакаёвай тэмпературы адбываецца вельмі павольна. Звычайна хуткасць рэакцыі паляпшаецца ў суровых умовах, такіх як высокая тэмпература і канцэнтраваны раствор гідраксіду натрыю.
Час публікацыі: 10 снежня 2024 г.