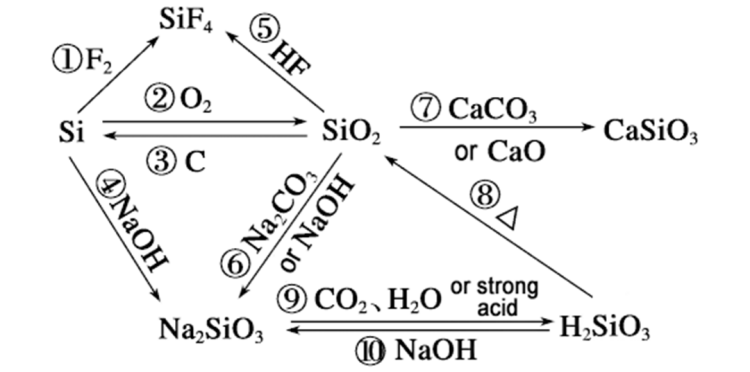
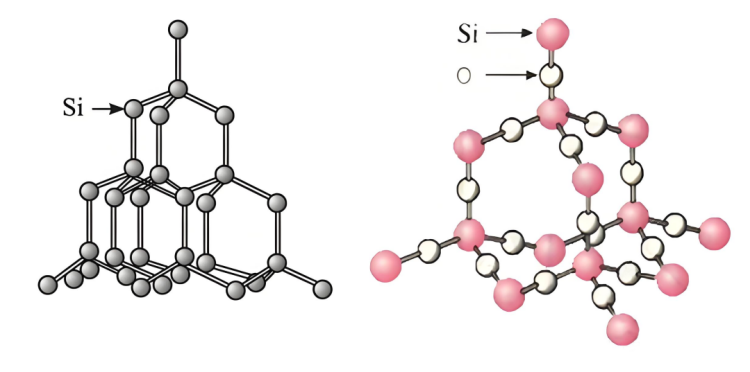
なぜ反応速度がシリコン水酸化ナトリウムが二酸化ケイ素を上回ることができる理由は、以下の側面から分析できます。
化学結合エネルギーの差
▪ ケイ素と水酸化ナトリウムの反応:ケイ素が水酸化ナトリウムと反応する際、ケイ素原子間のSi-Si結合エネルギーはわずか176kJ/molです。反応中にSi-Si結合が切断されますが、この結合は比較的切断されやすいため、速度論的に見ると、反応はより進行しやすいと言えます。
▪ 二酸化ケイ素と水酸化ナトリウムの反応:二酸化ケイ素中のケイ素原子と酸素原子間のSi-O結合エネルギーは460kJ/molと比較的高い。反応中にSi-O結合を切断するにはより高いエネルギーが必要となるため、反応は比較的起こりにくく、反応速度は遅い。
異なる反応機構
▪ シリコンは水酸化ナトリウムと反応します。シリコンはまず水酸化ナトリウムと反応し、水素とケイ酸を生成します。次にケイ酸は水酸化ナトリウムと反応し、ケイ酸ナトリウムと水を生成します。この反応中にシリコンと水の反応熱が発生し、分子運動が促進されます。これにより、反応にとってより良好な運動環境が形成され、反応速度が加速されます。
▪ 二酸化ケイ素は水酸化ナトリウムと反応します。二酸化ケイ素はまず水酸化ナトリウムと反応してケイ酸を生成し、次にケイ酸は水酸化ナトリウムと反応してケイ酸ナトリウムを生成します。二酸化ケイ素と水の反応は非常に遅く、反応過程では基本的に熱を発生しません。速度論的に見ると、急速な反応にはつながりません。
異なる材料構造
▪ シリコン構造:シリコン一定の結晶構造を持ち、原子間に一定の隙間があり、相互作用が比較的弱いため、水酸化ナトリウム溶液がシリコン原子と接触して反応しやすくなります。
▪ の構造シリコン二酸化炭素:シリコン二酸化炭素は安定した空間ネットワーク構造を持っています。シリコン二酸化ケイ素の原子と酸素原子は共有結合によって強固に結びつき、硬く安定した結晶構造を形成しています。水酸化ナトリウム溶液は二酸化ケイ素粒子の内部に浸透してケイ素原子に完全に接触することが難しく、迅速な反応が困難です。二酸化ケイ素粒子の表面にあるケイ素原子のみが水酸化ナトリウムと反応するため、反応速度が制限されます。
条件の影響
▪ シリコンと水酸化ナトリウムの反応: 加熱条件下では、シリコンと水酸化ナトリウム溶液の反応速度が大幅に加速され、一般的に高温でも反応がスムーズに進行します。
▪ 二酸化ケイ素と水酸化ナトリウムの反応:二酸化ケイ素と水酸化ナトリウム溶液の反応は室温では非常に遅いです。通常、高温や高濃度の水酸化ナトリウム溶液などの過酷な条件下では反応速度が向上します。
投稿日時: 2024年12月10日