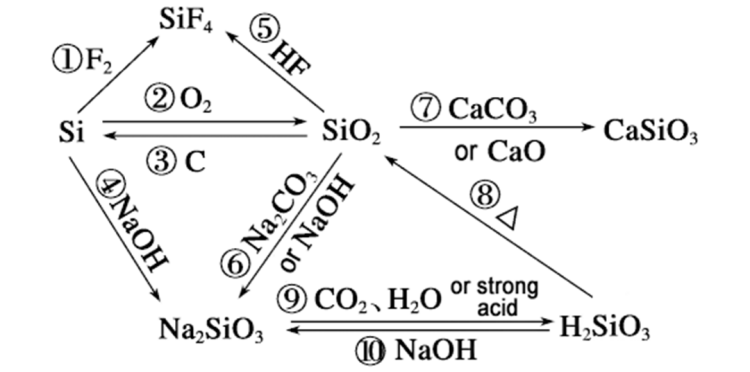
Por que a velocidade de reacción desilicioe o hidróxido de sodio pode superar o do dióxido de silicio e pódese analizar desde os seguintes aspectos:
Diferenza na enerxía de enlace químico
▪ Reacción do silicio e o hidróxido de sodio: Cando o silicio reacciona co hidróxido de sodio, a enerxía de enlace Si-Si entre os átomos de silicio é de só 176 kJ/mol. O enlace Si-Si rompe durante a reacción, o que é relativamente máis doado de romper. Desde un punto de vista cinético, a reacción é máis doada de levar a cabo.
▪ Reacción do dióxido de silicio e o hidróxido de sodio: a enerxía de enlace Si-O entre os átomos de silicio e os átomos de osíxeno no dióxido de silicio é de 460 kJ/mol, o que é relativamente alto. Necesítase máis enerxía para romper o enlace Si-O durante a reacción, polo que a reacción é relativamente difícil de producir e a velocidade de reacción é lenta.
Diferentes mecanismos de reacción
▪ O silicio reacciona co hidróxido de sodio: o silicio reacciona primeiro co hidróxido de sodio reaccionando coa auga para xerar hidróxeno e ácido silícico, e despois o ácido silícico reacciona co hidróxido de sodio para xerar silicato de sodio e auga. Durante esta reacción, a reacción entre o silicio e a auga libera calor, o que pode promover o movemento molecular, creando así un mellor ambiente cinético para a reacción e acelerando a velocidade de reacción.
▪ O dióxido de silicio reacciona co hidróxido de sodio: o dióxido de silicio reacciona primeiro co hidróxido de sodio reaccionando coa auga para xerar ácido silícico, e despois o ácido silícico reacciona co hidróxido de sodio para xerar silicato de sodio. A reacción entre o dióxido de silicio e a auga é extremadamente lenta e o proceso de reacción basicamente non libera calor. Desde un punto de vista cinético, non favorece unha reacción rápida.
Diferentes estruturas materiais
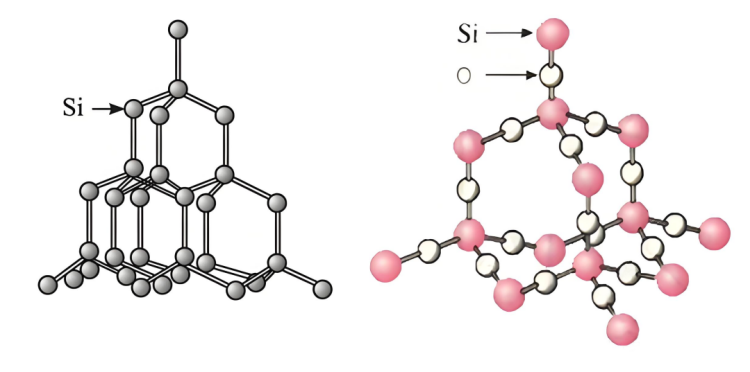
▪ Estrutura de silicio:Silicioten unha certa estrutura cristalina e existen certos ocos e interaccións relativamente débiles entre os átomos, o que facilita que a solución de hidróxido de sodio entre en contacto e reaccione cos átomos de silicio.
▪ Estrutura desiliciodióxido:silicioO dióxido ten unha estrutura de rede espacial estable.SilicioOs átomos de dióxido de silicio e os átomos de osíxeno están fortemente unidos por enlaces covalentes para formar unha estrutura cristalina dura e estable. É difícil que a solución de hidróxido de sodio penetre no seu interior e entre en contacto completo cos átomos de silicio, o que dificulta unha reacción rápida. Só os átomos de silicio na superficie das partículas de dióxido de silicio poden reaccionar co hidróxido de sodio, o que limita a velocidade de reacción.
Efecto das condicións
▪ Reacción do silicio co hidróxido de sodio: En condicións de quentamento, a velocidade de reacción do silicio coa solución de hidróxido de sodio acelerarase significativamente e a reacción pode xeralmente proceder sen problemas a altas temperaturas.
▪ Reacción do dióxido de silicio co hidróxido de sodio: A reacción do dióxido de silicio coa solución de hidróxido de sodio é moi lenta á temperatura ambiente. Normalmente, a velocidade de reacción mellora en condicións adversas, como altas temperaturas e solucións concentradas de hidróxido de sodio.
Data de publicación: 10 de decembro de 2024