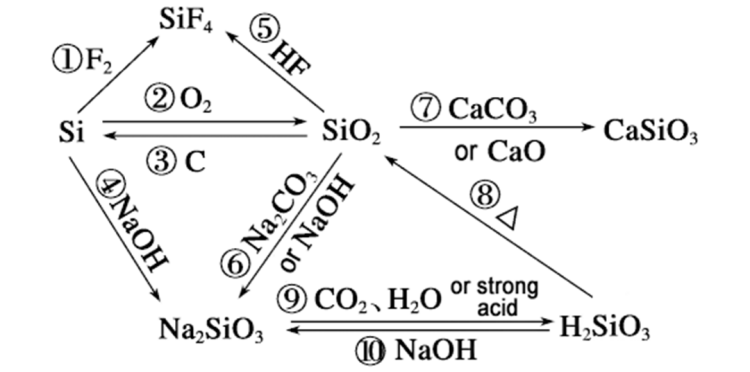
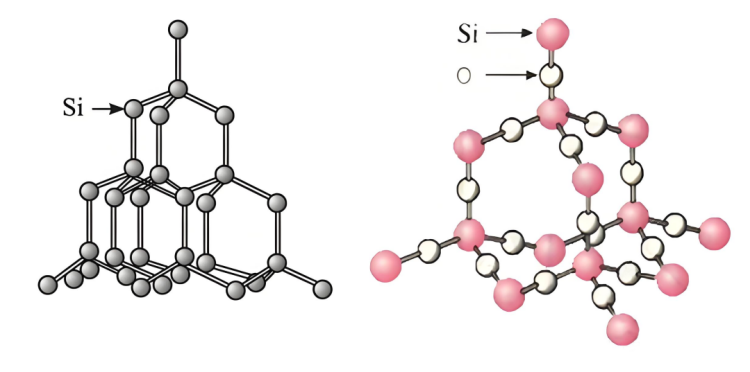
¿Por qué la velocidad de reacción desilicioy el hidróxido de sodio puede superar al dióxido de silicio y se puede analizar desde los siguientes aspectos:
Diferencia en la energía del enlace químico
▪ Reacción del silicio y el hidróxido de sodio: Cuando el silicio reacciona con el hidróxido de sodio, la energía del enlace Si-Si entre los átomos de silicio es de tan solo 176 kJ/mol. El enlace Si-Si se rompe durante la reacción, lo cual es relativamente más fácil de romper. Desde un punto de vista cinético, la reacción es más fácil de desarrollar.
▪ Reacción del dióxido de silicio y el hidróxido de sodio: La energía del enlace Si-O entre los átomos de silicio y los átomos de oxígeno en el dióxido de silicio es de 460 kJ/mol, una energía relativamente alta. Se requiere mayor energía para romper el enlace Si-O durante la reacción, por lo que esta es relativamente difícil de producir y la velocidad de reacción es lenta.
Diferentes mecanismos de reacción
▪ El silicio reacciona con el hidróxido de sodio: El silicio reacciona primero con el hidróxido de sodio al reaccionar con agua para generar hidrógeno y ácido silícico, y luego el ácido silícico reacciona con el hidróxido de sodio para generar silicato de sodio y agua. Durante esta reacción, la interacción entre el silicio y el agua libera calor, lo que puede promover el movimiento molecular, creando así un mejor entorno cinético para la reacción y acelerando su velocidad.
El dióxido de silicio reacciona con el hidróxido de sodio: El dióxido de silicio reacciona primero con el hidróxido de sodio al reaccionar con agua para generar ácido silícico, y luego con el hidróxido de sodio para generar silicato de sodio. La reacción entre el dióxido de silicio y el agua es extremadamente lenta y prácticamente no libera calor. Desde un punto de vista cinético, no favorece una reacción rápida.
Diferentes estructuras de materiales
▪ Estructura de silicio:SilicioTiene una estructura cristalina determinada y existen ciertos espacios e interacciones relativamente débiles entre los átomos, lo que hace más fácil que la solución de hidróxido de sodio entre en contacto y reaccione con los átomos de silicio.
▪ Estructura desiliciodióxido:silicioEl dióxido tiene una estructura de red espacial estable.SilicioLos átomos de silicio y los átomos de oxígeno están estrechamente unidos mediante enlaces covalentes para formar una estructura cristalina dura y estable. Es difícil que la solución de hidróxido de sodio penetre en su interior y entre en contacto completo con los átomos de silicio, lo que dificulta una reacción rápida. Solo los átomos de silicio en la superficie de las partículas de dióxido de silicio pueden reaccionar con el hidróxido de sodio, lo que limita la velocidad de reacción.
Efecto de las condiciones
▪ Reacción del silicio con hidróxido de sodio: en condiciones de calentamiento, la velocidad de reacción del silicio con la solución de hidróxido de sodio se acelerará significativamente y la reacción generalmente puede continuar sin problemas a altas temperaturas.
Reacción del dióxido de silicio con hidróxido de sodio: La reacción del dióxido de silicio con una solución de hidróxido de sodio es muy lenta a temperatura ambiente. Normalmente, la velocidad de reacción mejora en condiciones adversas, como altas temperaturas y una solución concentrada de hidróxido de sodio.
Hora de publicación: 10 de diciembre de 2024